Page 37 -
P. 37
на кінетику десорбції гідриду. Показано, що Ti та Fe може синергетично каталі-
зувати сорбцію водню магнієм, де Fe діє як каталізатор, а Ti, утворюючи гідрид
титану, діє як агент регулювання розміру, запобігаючи агломерації та спіканню
частинок Mg. Також ці покращення пов’язані з можливим утворенням нанокри-
сталічної/аморфної фази TiFe [72, 85].
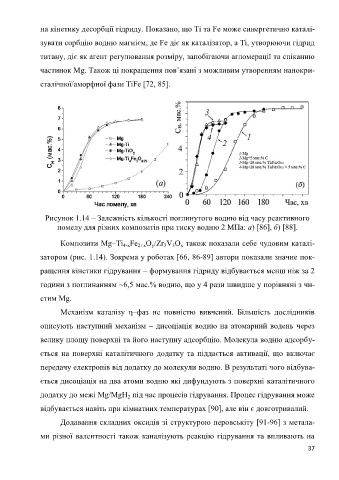
Рисунок 1.14 – Залежність кількості поглинутого водню від часу реактивного
помелу для різних композитів при тиску водню 2 МПа: а) [86], б) [88].
Композити Mg–Ti Fe 2+x O /Zr V O також показали себе чудовим каталі-
4-x
3
3
x
y
затором (рис. 1.14). Зокрема у роботах [66, 86-89] автори показали значне пок-
ращення кінетики гідрування – формування гідриду відбувається менш ніж за 2
години з поглинанням ~6,5 мас.% водню, що у 4 рази швидше у порівняні з чи-
стим Mg.
Механізм каталізу η–фаз не повністю вивчений. Більшість дослідників
описують наступний механізм – дисоціація водню на атомарний водень через
велику площу поверхні та його наступну адсорбцію. Молекула водню адсорбу-
ється на поверхні каталітичного додатку та піддається активації, що включає
передачу електронів від додатку до молекули водню. В результаті чого відбува-
ється дисоціація на два атоми водню які дифундують з поверхні каталітичного
додатку до межі Mg/MgH під час процесів гідрування. Процес гідрування може
2
відбувається навіть при кімнатних температурах [90], але він є довготривалий.
Додавання складних оксидів зі структурою перовськіту [91-96] з метала-
ми різної валентності також каналізують реакцію гідрування та впливають на
37