Page 101 -
P. 101
1200 1 H2O 6 78,3
MgCl2 моль/л 5
2 0,01 4
1000 3 0,03 65,2
4 0,05 3 52,2
5 0,07
800
V(H 2 ), мл/г 400 1 26,1
600 6 0,1 2 39,1 Конверсія, %
200 13
0
0 600 1200 1800
, c
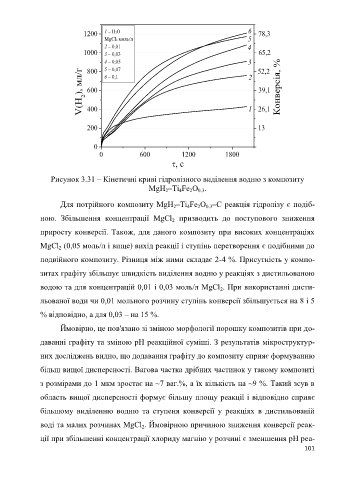
Рисунок 3.31 – Кінетичні криві гідролізного виділення водню з композиту
MgH –Ti Fe O .
4
0.3
2
2
Для потрійного композиту MgH –Ti Fe O –C реакція гідролізу є подіб-
4
2
0.3
2
ною. Збільшення концентрації MgCl призводить до поступового зниження
2
приросту конверсії. Також, для даного композиту при високих концентраціях
MgCl (0,05 моль/л і вище) вихід реакції і ступінь перетворення є подібними до
2
подвійного композиту. Різниця між ними складає 2-4 %. Присутність у компо-
зитах графіту збільшує швидкість виділення водню у реакціях з дистильованою
водою та для концентрацій 0,01 і 0,03 моль/л MgCl . При використанні дисти-
2
льованої води чи 0,01 мольного розчину ступінь конверсії збільшується на 8 і 5
% відповідно, а для 0,03 – на 15 %.
Ймовірно, це пов'язано зі зміною морфології порошку композитів при до-
даванні графіту та зміною рН реакційної суміші. З результатів мікроструктур-
них досліджень видно, що додавання графіту до композиту сприяє формуванню
більш вищої дисперсності. Вагова частка дрібних частинок у такому композиті
з розмірами до 1 мкм зростає на ~7 ваг.%, а їх кількість на ~9 %. Такий зсув в
область вищої дисперсності формує більшу площу реакції і відповідно сприяє
більшому виділенню водню та ступеня конверсії у реакціях в дистильованій
воді та малих розчинах MgCl . Ймовірною причиною зниження конверсії реак-
2
ції при збільшенні концентрації хлориду магнію у розчині є зменшення pH реа-
101