Page 77 -
P. 77
1200 81
1 H2O 4
MgCl2 моль/л
1000 2 0,01 3 67,5
3 0,03
800 4 0,04 54 Конверсія, %
V(H 2 ), мл/г 600 2 40,5
1
27
400
200 13,5
0
0 600 1200 1800
, c
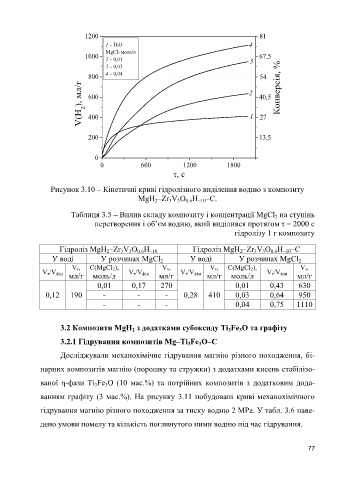
Рисунок 3.10 – Кінетичні криві гідролізного виділення водню з композиту
MgH –Zr V O H –C.
~10
0.6
3
2
3
Таблиця 3.5 – Вплив складу композиту і концентрації MgCl на ступінь
2
перетворення і об’єм водню, який виділився протягом τ = 2000 с
гідролізу 1 г композиту
Гідроліз MgH –Zr V O H Гідроліз MgH –Zr V O H –C
3
3
2
0.6
2
~10
0.6
~10
3
3
У воді У розчинах MgCl У воді У розчинах MgCl
2
2
V τ, C(MgCl 2), V τ, V τ, C(MgCl 2), V τ,
V τ/V фін V τ/V фін V τ/V фін V τ/V фін
мл/г моль/л мл/г мл/г моль/л мл/г
0,01 0,17 270 0,01 0,43 630
0,12 190 - - - 0,28 410 0,03 0,64 950
- - - 0,04 0,75 1110
3.2 Композити MgH з додатками субоксиду Ti Fe O та графіту
3
3
2
3.2.1 Гідрування композитів Mg–Ti Fe O–С
3
3
Досліджували механохімічне гідрування магнію різного походження, бі-
нарних композитів магнію (порошку та стружки) з додатками кисень стабілізо-
ваної η-фази Ti Fe O (10 мас.%) та потрійних композитів з додатковим дода-
3
3
ванням графіту (3 мас.%). На рисунку 3.11 побудовані криві механохімічного
гідрування магнію різного походження за тиску водню 2 MPa. У табл. 3.6 наве-
дено умови помелу та кількість поглинутого ними водню під час гідрування.
77