Page 89 -
P. 89
ляє досягнути конверсії у 82 % з виділенням 1260 мл водню з 1 граму компози-
ту. Подальше зростання концентрації хлориду магнію спричиняє різке знижен-
ня конверсії реакції. Також, на рис. 3.19 можна побачити нерівномірний харак-
тер перебігу реакції, ймовірно, через присутність конгломератів порошку які не
одразу розчиняються у розчині через поверхневі явища.
6 5
1200 1 H2O 81
MgCl2 моль/л 4
2 0,01 3
1000 3 0,03 67,5
4 0,05 2
), мл/г 800 6 0,1 1 54 Конверсія, %
5 0,07
V(H 2 600 40,5
400 27
200 13,5
0
0 600 1200 1800
, с
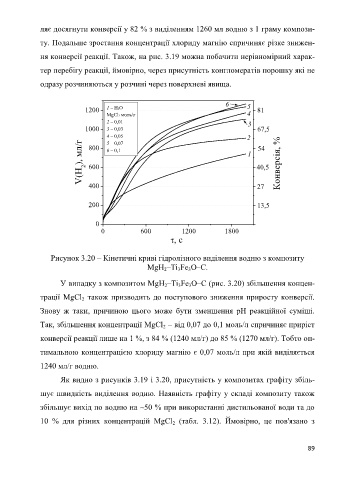
Рисунок 3.20 – Кінетичні криві гідролізного виділення водню з композиту
MgH –Ti Fe O–C.
3
2
3
У випадку з композитом MgH –Ti Fe O–C (рис. 3.20) збільшення концен-
2
3
3
трації MgCl також призводить до поступового зниження приросту конверсії.
2
Знову ж таки, причиною цього може бути зменшення pH реакційної суміші.
Так, збільшення концентрації MgCl – від 0,07 до 0,1 моль/л спричиняє приріст
2
конверсії реакції лише на 1 %, з 84 % (1240 мл/г) до 85 % (1270 мл/г). Тобто оп-
тимальною концентрацією хлориду магнію є 0,07 моль/л при якій виділяється
1240 мл/г водню.
Як видно з рисунків 3.19 і 3.20, присутність у композитах графіту збіль-
шує швидкість виділення водню. Наявність графіту у складі композиту також
збільшує вихід по водню на ~50 % при використанні дистильованої води та до
10 % для різних концентрацій MgCl (табл. 3.12). Ймовірно, це пов'язано з
2
89