Page 28 -
P. 28
Другий та наступні цикли гідрування проходять на порядок швидше, але
все ще залежать від тиску [17]. Так, 80–90% магнію перетворюється в гідрид за
2…20 годин при тиску водню 2…4 МПа та температури 300…400 °С і потім
реакція практично зупиняється [19, 22, 23]. Такі відмінності в кінетичних хара-
ктеристиках спричинені тим, що поверхневий шар оксиду/гідроксиду магнію,
який інгібує абсорбцію водню [20], після першого циклу значно скорочується, а
тріщини, утворені гідридом, збільшують площу частинки.
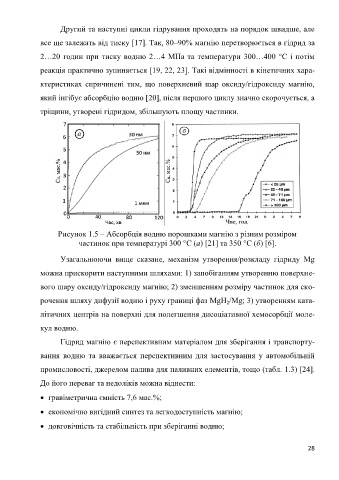
Рисунок 1.5 – Абсорбція водню порошками магнію з різним розміром
частинок при температурі 300 °С (a) [21] та 350 °С (б) [6].
Узагальнюючи вище сказане, механізм утворення/розкладу гідриду Mg
можна прискорити наступними шляхами: 1) запобіганням утворенню поверхне-
вого шару оксиду/гідроксиду магнію; 2) зменшенням розміру частинок для ско-
рочення шляху дифузії водню і руху границі фаз MgH /Mg; 3) утворенням ката-
2
літичних центрів на поверхні для полегшення дисоціативної хемосорбції моле-
кул водню.
Гідрид магнію є перспективним матеріалом для зберігання і транспорту-
вання водню та вважається перспективним для застосування у автомобільній
промисловості, джерелом палива для паливних елементів, тощо (табл. 1.3) [24].
До його переваг та недоліків можна віднести:
гравіметрична ємність 7,6 мас.%;
економічно вигідний синтез та легкодоступність магнію;
довговічність та стабільність при зберіганні водню;
28