Page 13 - Avtoreferat Voloshyn 2020
P. 13
13
їх хемосорбційної взаємодії з поверхневими атомами феруму, пасиваційними
властивостями нітрит- та хромат-іонів, а також протекторною дією іонів цинку.
Досліджено вплив складу водного середовища на період зародження корозійно-
втомної тріщини N i та характеристики відновлення рівноважного стану металу
свіжодеформованої поверхні сталі 17Г1С (інтенсивність розчинення ювенільного
металу деформованої поверхні І 0, швидкість спаду струму S та кількість електрики на
окиснення металу свіжодеформованої поверхні q за потенціалу поляризації, рівного
потенціалу корозії). За базове середовище використали 0,01 N розчин NaHCO 3 з
-
2-
2-
додатками аніонів Сl (0,005 N), SO 4 (0,003 N), CO 3 (0,005 N), PO 4 (0,005 N), NO 3
-
3-
(0,005 N) та ОН (рН = 11) за природної аерації.
-
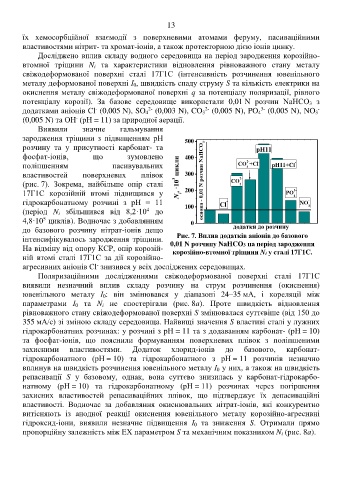
Виявили значне гальмування
зародження тріщини з підвищенням рН 500
розчину та у присутності карбонат- та pH11
фосфат-іонів, що зумовлено 400
2-
поліпшенням пасивувальних CO +Cl - pH11+Cl -
3
властивостей поверхневих плівок N і , ·10 3 цикли 300 2-
(рис. 7). Зокрема, найбільше опір сталі основа - 0,01 N розчин NaHCO 3 CO 3
17Г1С корозійній втомі підвищився у 200 PO 3-
4
гідрокарбонатному розчині з рН = 11 100 Cl - NO - 3
(період N і збільшився від 8,2·10 до
4
4,8·10 циклів). Водночас з добавлянням 0
5
до базового розчину нітрат-іонів дещо додатки до розчину
інтенсифікувалось зародження тріщини. Рис. 7. Вплив додатків аніонів до базового
На відміну від опору КСР, опір корозій- 0,01 N розчину NaHCO3 на період зародження
корозійно-втомної тріщини Nі у сталі 17Г1С.
ній втомі сталі 17Г1С за дії корозійно-
-
агресивних аніонів Сl знизився у всіх досліджених середовищах.
Поляризаційними дослідженнями свіжодеформованої поверхні сталі 17Г1С
виявили незначний вплив складу розчину на струм розчинення (окиснення)
ювенільного металу І 0: він змінювався у діапазоні 24–35 мА, і кореляції між
параметрами І 0 та N i не спостерігали (рис. 8а). Проте швидкість відновлення
рівноважного стану свіжодеформованої поверхні S змінювалася суттєвіше (від 150 до
355 мА/с) зі зміною складу середовища. Найвищі значення S властиві сталі у лужних
гідрокарбонатних розчинах: у розчині з рН = 11 та з додаванням карбонат- (рН = 10)
та фосфат-іонів, що пояснили формуванням поверхневих плівок з поліпшеними
захисними властивостями. Додаток хлорид-іонів до базового, карбонат-
гідрокарбонатного (рН = 10) та гідрокарбонатного з рН = 11 розчинів незначно
вплинув на швидкість розчинення ювенільного металу І 0 у них, а також на швидкість
репасивації S у базовому, однак, вона суттєво знизилась у карбонат-гідрокарбо-
натному (рН = 10) та гідрокарбонатному (рН = 11) розчинах через погіршення
захисних властивостей репасиваційних плівок, що підтверджує їх депасиваційні
властивості. Водночас за добавляння окиснювальних нітрат-іонів, які конкурентно
витісняють із анодної реакції окиснення ювенільного металу корозійно-агресивні
гідроксид-іони, виявили незначне підвищення І 0 та зниження S. Отримали прямо
пропорційну залежність між ЕХ параметром S та механічним показником N i (рис. 8а).