Page 12 - Avtoreferat Voloshyn 2020
P. 12
12
Таблиця 2. ЕХ характеристики сталі 17Г1С у водних середовищах різного складу
2
2
Корозивне середовище –Ecorr, В іcorr, мкА/cм Rp, кОмcм
0,01 N NaHCO3, деаерований N2 0,565 9,4 2,58
0,01 N NaHCO3 + О2 (аерований) 0,588 12,1 2,06
0,01 N NaHCO3 + 0,005 N СО3 0,819 6,2 3,40
2-
-
0,01 N NaHCO3 + 0,005 N Cl 0,612 32,6 0,66
3-
0,01 N NaHCO3 + 0,005 N PO4 0,765 7,9 3,01
Виявили відсутність кореляції між характерис- 20
тиками опору сталі 17Г1С виразковій корозії k p , % 0,01 N HCO 3 - +Cl -
та КСР λ (рис. 6). Отже, гіпотеза про утворення
корозійного пошкодження як необхідної умови 15 3-
для зародження корозійно-механічної тріщини +PO 4
не підтвердилась. Таким чином, схильність +O +O +Cl -
2
сталі 17Г1С до КСР у 0,01 N NaHCO 3 зростає із 10 2
посиленням катодної поляризації, не залежить -
від інтенсивності виразкової корозії (наявності 5 +NO 3
-
іонів Cl ) та знижується із гальмуванням виділе-
ння водню внаслідок як конкурентної адсорбції +CO 2- +CO +Cl -
2-
3
-
(наявності О 2, NO 3 ), так і зростання бар`єрних 0 3
6
характеристик плівок продуктів корозії 0 3 k , см -2 9 12
3-
2-
(наявності О 2, РО 4 , СО 3 ). Тому водневе p
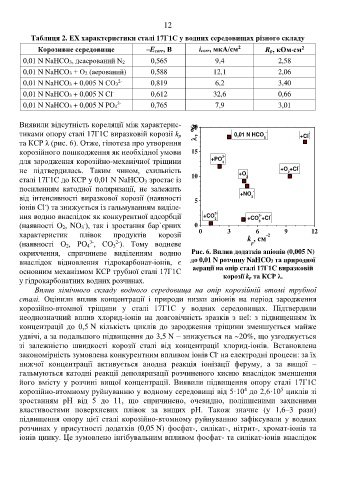
окрихчення, спричинене виділенням водню Рис. 6. Вплив додатків аніонів (0,005 N)
внаслідок відновлення гідрокарбонат-іонів, є до 0,01 N розчину NaHCO3 та природної
основним механізмом КСР трубної сталі 17Г1С аерації на опір сталі 17Г1С виразковій
у гідрокарбонатних водних розчинах. корозії kp та КСР λ.
Вплив хімічного складу водного середовища на опір корозійній втомі трубної
сталі. Оцінили вплив концентрації і природи низки аніонів на період зародження
корозійно-втомної тріщини у сталі 17Г1С у водних середовищах. Підтвердили
неоднозначний вплив хлорид-іонів на довговічність зразків з неї: з підвищенням їх
концентрації до 0,5 N кількість циклів до зародження тріщини зменшується майже
удвічі, а за подальшого підвищення до 3,5 N – знижується на 20%, що узгоджується
зі залежністю швидкості корозії сталі від концентрації хлорид-іонів. Встановлена
закономірність зумовлена конкурентним впливом іонів Cl на електродні процеси: за їх
-
нижчої концентрації активується анодна реакція іонізації феруму, а за вищої –
гальмуються катодні реакції деполяризації розчиненого кисню внаслідок зменшення
його вмісту у розчині вищої концентрації. Виявили підвищення опору сталі 17Г1С
4
5
корозійно-втомному руйнуванню у водному середовищі від 5·10 до 2,6·10 циклів зі
зростанням рН від 5 до 11, що спричинено, очевидно, поліпшеними захисними
властивостями поверхневих плівок за вищих рН. Також значне (у 1,6–3 рази)
підвищення опору цієї сталі корозійно-втомному руйнуванню зафіксували у водних
розчинах у присутності додатків (0,05 N) фосфат-, силікат-, нітрит-, хромат-іонів та
іонів цинку. Це зумовлено інгібувальним впливом фосфат- та силікат-іонів внаслідок