Page 63 - дисертація головей3-converted
P. 63
64
У розчині 0,5 % CH 3COOH + 5 % NaCl струми корозії збільшуються ~2,3
та ~2,6 рази порівняно з 5% NaCl та 0,5 % CH 3COOH, відповідно (табл.3.1).
Потенціал корозії Е кор=-376 мВ, і є додатнішим, ніж у 5% NaCl та від’ємнішим,
ніж 0,5 % CH 3COOH. За перенапруги η=50 мВ ефективність анодних процесів
зростає в ~1,6 і ~4,4, а катодних −в ~3,2 і ~1,5 рази порівняно з розчином натрій
хлориду та ацетатної кислоти, відповідно (рис.3.9, криві 1, 3, 5). Корозія
перетікає за катодного контролю. Отже, спільна дія хлорид- та ацетат- іонів
зменшує перенапругу виділення водню [105].
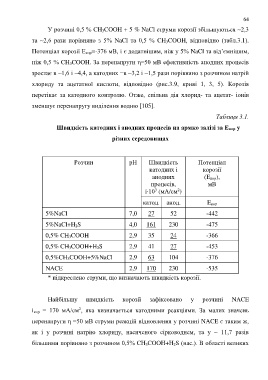
Таблиця 3.1.
Швидкість катодних і анодних процесів на армко залізі за Екор у
різних середовищах
Розчин рН Швидкість Потенціал
катодних і корозії
анодних (Е кор),
процесів, мВ
3
2
i∙10 (мA/см )
катод. анод. E кор
5%NaCl 7,0 27 52 -442
5%NaCl+H 2S 4,0 161 230 -475
0,5% CH 3COOH 2,9 35 24 -366
0,5% CH 3COOH+H 2S 2,9 41 27 -453
0,5%CH 3COOH+5%NaCl 2,9 63 104 -376
NACE 2,9 170 230 -535
* підкреслено струми, що визначають швидкість корозії.
Найбільшу швидкість корозії зафіксовано у розчині NACE
2
і кор = 170 мA/см , яка визначається катодними реакціями. За малих значень
перенапруги η =50 мВ струми реакцій відновлення у розчині NACE є таким ж,
як і у розчині натрію хлориду, насиченого сірководнем, та у ~ 11,7 разів
більшими порівняно з розчином 0,5% CH 3COOH+H 2S (нас.). В області великих